Pesquisadores descobriram que as bactérias e fungos responsáveis por uma forma grave de cárie dentária na infância formam, juntos, “superorganismos” com propriedades inesperadas. Os agrupamentos entre reinos foram mais resistentes a antimicrobianos e remoção física do que qualquer uma das espécies sozinhas, brotando ‘membros’ para se mover como um grupo e se espalhar rapidamente nos dentes.
Por Universidade da Pensilvânia com informações de Science Daily.
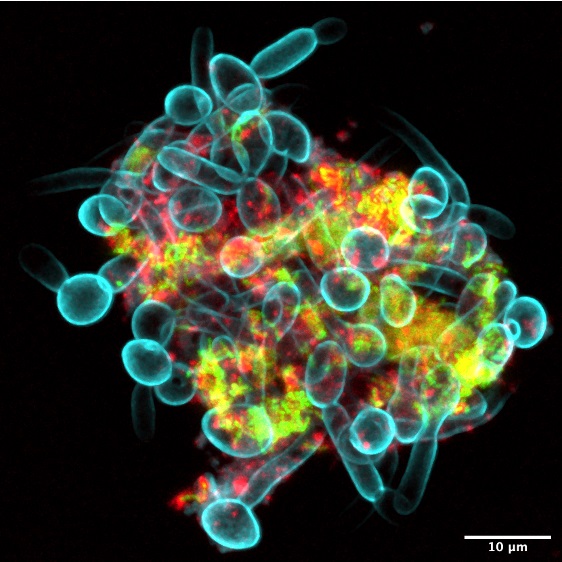
Uma parceria entre os reinos entre bactérias e fungos pode resultar na união dos dois para formar um “superorganismo” com força e resiliência incomuns. Pode parecer coisa de ficção científica, mas esses agrupamentos microbianos fazem parte do aqui e agora.
Encontrados na saliva de crianças com cárie dentária grave na infância, esses conjuntos podem efetivamente colonizar os dentes. Eles eram mais pegajosos, mais resistentes a antimicrobianos e mais difíceis de remover dos dentes do que as bactérias ou os fungos sozinhos, de acordo com a equipe de pesquisa, liderada por cientistas da Escola de Medicina Dentária da Universidade da Pensilvânia.
Além do mais, os conjuntos inesperadamente brotam “membros” que os impulsionam a “andar” e “saltar” para se espalhar rapidamente na superfície do dente, apesar de cada micróbio por si só não ser móvel, relatou a equipe na revista Proceedings of the National Academia de Ciências .
“Isso começou com uma descoberta muito simples, quase acidental, ao analisar amostras de saliva de crianças que desenvolvem cáries dentárias agressivas”, diz Hyun (Michel) Koo, professor da Penn Dental Medicine e autor co-correspondente do artigo. “Olhando sob o microscópio, notamos as bactérias e fungos formando esses conjuntos e desenvolvendo movimentos que nunca pensamos que eles teriam: uma mobilidade ‘como andar’ e ‘como pular’. Eles têm muito do que chamamos de ‘funções emergentes’, que trazem novos benefícios a esse conjunto que eles não poderiam alcançar sozinhos. É quase como um novo organismo – um superorganismo – com novas funções.”
Melhor (ou pior) juntos
No passado, o laboratório de Koo se concentrou no biofilme dental, ou placa, presente em crianças com cáries dentárias graves, descobrindo que ambas as bactérias – Streptococcus mutans – e fungos – Candida albicans – contribuem para a doença. A cárie, comumente conhecida como cárie, surge quando os açúcares da dieta permanecem para alimentar bactérias e fungos na boca, levando à placa dentária produtora de ácido que destrói o esmalte.
O novo conjunto de descobertas surgiu quando Zhi Ren, um pós-doutorando do grupo de Koo, estava usando microscopia que permite aos cientistas visualizar o comportamento de micróbios vivos em tempo real. A técnica “abre novas possibilidades para investigar a dinâmica de processos biológicos complexos”, diz Ren, primeiro autor do artigo e parte da primeira coorte do programa de treinamento de pós-doutorado NIDCR T90R90 no Centro de Inovação e Odontologia de Precisão da Penn.
Depois de ver os aglomerados de bactérias e fungos presentes nas amostras de saliva, Ren, Koo e colegas ficaram curiosos sobre como os agrupamentos poderiam se comportar uma vez presos à superfície de um dente. Assim começou uma série de experimentos usando microscopia ao vivo em tempo real para observar o processo de fixação e eventual crescimento.
Eles criaram um sistema de laboratório para recriar a formação desses conjuntos, usando bactérias, fungos e um material semelhante a um dente, todos incubados na saliva humana. A plataforma permitiu que os pesquisadores observassem os agrupamentos se reunindo e analisassem a estrutura dos conjuntos resultantes. Eles encontraram uma estrutura altamente organizada com aglomerados bacterianos ligados em uma rede complexa de leveduras fúngicas e projeções semelhantes a filamentos chamadas hifas, todas enredadas em um polímero extracelular, um material semelhante a cola.
Em seguida, a equipe testou as propriedades desses conjuntos entre reinos, uma vez que colonizaram a superfície do dente e encontraram “comportamentos surpreendentes e propriedades emergentes”, diz Ren, “incluindo adesão de superfície aprimorada, tornando-os muito pegajosos e maior tolerância mecânica e antimicrobiana, tornando-os difíceis de remover ou matar.”
Talvez a característica mais intrigante dos conjuntos, dizem os pesquisadores, seja sua mobilidade. “Eles exibiam movimentos de ‘pular’ e ‘andar’ enquanto cresciam continuamente”, diz Ren.
Enquanto algumas bactérias podem se impulsionar usando apêndices como flagelos, as espécies microbianas no estudo atual são imóveis. E, diferentemente de qualquer motilidade microbiana conhecida, as assembléias usaram as hifas fúngicas para ancorar na superfície e, em seguida, impulsionar todo o superorganismo para a frente, transportando as bactérias anexadas pela superfície, diz Koo, “como bactérias pegando carona nos fungos”.
Os agrupamentos microbianos se moveram rápido e longe, descobriram os pesquisadores. Na superfície semelhante a um dente, a equipe mediu velocidades de mais de 40 mícrons por hora, semelhante à velocidade dos fibroblastos, um tipo de célula do corpo humano envolvida na cicatrização de feridas. Nas primeiras horas de crescimento, os cientistas observaram os conjuntos “saltando” mais de 100 mícrons pela superfície. “Isso é mais de 200 vezes o comprimento do seu próprio corpo”, diz Ren, “tornando-os ainda melhores do que a maioria dos vertebrados, em relação ao tamanho do corpo. Por exemplo, pererecas e gafanhotos podem saltar para a frente cerca de 50 vezes e 20 vezes o comprimento do seu próprio corpo. , respectivamente.”
Embora os mecanismos exatos sejam desconhecidos, a capacidade dos conjuntos de “se mover à medida que crescem”, dizem os pesquisadores, tem uma consequência clara: permite que eles colonizem e se espalhem rapidamente para novas superfícies. Quando a equipe de pesquisa permitiu que os conjuntos se fixassem e crescessem em dentes humanos reais em um modelo de laboratório, eles encontraram cáries mais extensas como resultado de um biofilme que se espalhava rapidamente.
Tratamento de doenças e biologia em geral
Como esses conjuntos são encontrados na saliva, direcioná-los desde o início pode ser uma estratégia terapêutica para prevenir a cárie dentária na infância, diz Koo. “Se você bloquear essa ligação ou interromper a montagem antes que ela chegue ao dente e cause danos, isso pode ser uma estratégia preventiva”.
E além das aplicações para o tratamento dessa doença específica, dizem os pesquisadores, as novas descobertas podem ser aplicáveis na biologia microbiana em geral. Por exemplo, organismos agregados encontrados em outros fluidos biológicos ou ecossistemas aquáticos podem, da mesma forma, aumentar a colonização e o crescimento da superfície para causar doenças infecciosas ou contaminação ambiental.
“Vimos que esses dois organismos distintos se reúnem como uma nova entidade orgânica que deu a cada um benefícios e funções adicionais que as células únicas não tinham por conta própria”, diz Koo. As descobertas podem até esclarecer a evolução do mutualismo e da multicelularidade que aumenta a sobrevivência e o crescimento de organismos únicos quando eles se unem e trabalham juntos como uma unidade em um determinado ambiente, observa a equipe.
“Esta descoberta de um superorganismo ‘bandido’ é realmente inovadora e imprevista”, diz Knut Drescher, da Universidade de Basel, autor co-correspondente do artigo. “Ninguém teria previsto isso. Zhi acidentalmente se deparou com isso mantendo a mente aberta.”
Hyun (Michel) Koo é professor do Departamento de Ortodontia e das divisões de Saúde Bucal Comunitária e Odontopediatria da Faculdade de Medicina Dentária e cofundador do Centro de Inovação e Odontologia de Precisão (CiPD) da Universidade da Pensilvânia .
Zhi Ren é membro do programa de treinamento de pós-doutorado do Instituto Nacional de Pesquisa Odontológica e Craniofacial T90/R90 Treinamento Avançado na Interface de Engenharia e Ciências Orais-Craniofaciais no CiPD na Escola de Medicina Dentária da Penn e na Escola de Engenharia e Ciências Aplicadas. Ren também foi bolsista de odontopediatria da Colgate-Palmolive (2019-21).
Knut Drescher é professor associado do Biozentrum da Universidade de Basel, na Suíça.
Os coautores de Koo e Ren no papel foram Aurea Simon-Soro da Penn Dental Medicine, Zhenting Xiang, Yuan Liu e Indira M. Cavalcanti; Hannah Jeckel, da Philipps-Universität Marburg; Jin Xiao, da Universidade de Rochester Medical Center; Nyi-Nyi Tin e Anderson Hara da Universidade de Indiana; e Knut Drescher da Universidade de Basileia. Ren e Jeckel compartilharam a primeira autoria, e Drescher e Koo foram autores co-correspondentes.
Este trabalho foi apoiado em parte pelo Instituto Nacional de Pesquisa Odontológica e Craniofacial (bolsas DE025220 e DE031532), o Budesministerium für Bildung und Forschung (Grant TARGET-Biofilm) e o Conselho Europeu de Pesquisa (Grant 716743).
Fonte da história:
Materiais fornecidos pela Universidade da Pensilvânia. Original escrito por Katherine Unger Baillie.
Referência do jornal :
Zhi Ren, Hannah Jeckel, Aurea Simon-Soro, Zhenting Xiang, Yuan Liu, Indira M. Cavalcanti, Jin Xiao, Nyi-Nyi Tin, Anderson Hara, Knut Drescher, Hyun Koo. Interkingdom assemblages in human saliva display group-level surface mobility and disease-promoting emergent functions. Proceedings of the National Academy of Sciences, 2022; 119 (41) DOI: 10.1073/pnas.2209699119