As propriedades da ‘Lipocartilagem’ são semelhantes às do material de embalagem com bolhas — superestável, macio e elástico.
Por Universidade da Califórnia – Irvine, com informações de Science Daily.
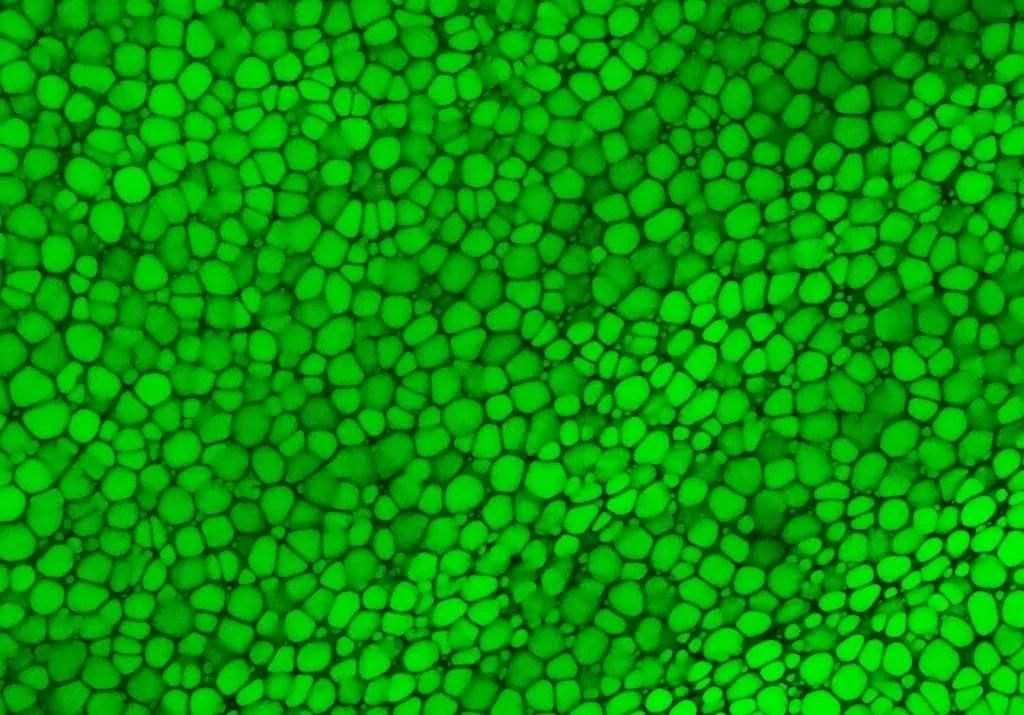
Uma equipe de pesquisa internacional liderada pela Universidade da Califórnia, Irvine, descobriu um novo tipo de tecido esquelético que oferece grande potencial para o avanço da medicina regenerativa e da engenharia de tecidos.
A maior parte da cartilagem depende de uma matriz extracelular externa para sua resistência, mas a “lipocartilagem”, encontrada nas orelhas, nariz e garganta dos mamíferos, é exclusivamente repleta de células cheias de gordura chamadas “lipocondrócitos”, que fornecem suporte interno superestável, permitindo que o tecido permaneça macio e elástico — semelhante ao material de embalagem com bolhas.
O estudo, publicado online no periódico Science, descreve como as células da lipocartilagem criam e mantêm seus próprios reservatórios lipídicos, permanecendo constantes em tamanho. Ao contrário das células de gordura dos adipócitos comuns, os lipocondrócitos nunca encolhem ou expandem em resposta à disponibilidade de alimentos.
“A resiliência e estabilidade da lipocartilagem fornecem uma qualidade elástica e complacente que é perfeita para partes flexíveis do corpo, como lóbulos das orelhas ou a ponta do nariz, abrindo possibilidades interessantes na medicina regenerativa e engenharia de tecidos, particularmente para defeitos faciais ou lesões”, disse o autor correspondente Maksim Plikus, professor de biologia celular e do desenvolvimento da UC Irvine. “Atualmente, a reconstrução da cartilagem geralmente requer a coleta de tecido da costela do paciente — um procedimento doloroso e invasivo. No futuro, lipocondrócitos específicos do paciente podem ser derivados de células-tronco, purificados e usados para fabricar cartilagem viva adaptada às necessidades individuais. Com a ajuda da impressão 3D, esses tecidos projetados podem ser moldados para se encaixar precisamente, oferecendo novas soluções para tratar defeitos congênitos, traumas e várias doenças da cartilagem.”
O Dr. Franz Leydig reconheceu os lipocondrócitos pela primeira vez em 1854, quando notou a presença de gotículas de gordura na cartilagem das orelhas de ratos, uma descoberta que foi amplamente esquecida até agora. Com ferramentas bioquímicas modernas e métodos de imagem avançados, os pesquisadores da UC Irvine caracterizaram de forma abrangente a biologia molecular, o metabolismo e o papel estrutural da lipocartilagem nos tecidos esqueléticos.
Eles também descobriram o processo genético que suprime a atividade de enzimas que quebram gorduras e reduzem a absorção de novas moléculas de gordura, efetivamente bloqueando as reservas lipídicas dos lipocondrócitos no lugar. Quando despojada de seus lipídios, a lipocartilagem se torna rígida e quebradiça, destacando a importância de suas células cheias de gordura na manutenção da combinação de durabilidade e flexibilidade do tecido. Além disso, a equipe observou que em alguns mamíferos, como morcegos, os lipocondrócitos se reúnem em formas intrincadas, como cristas paralelas em suas orelhas grandes, o que pode aumentar a acuidade auditiva modulando as ondas sonoras.
“A descoberta da biologia lipídica única da lipocartilagem desafia suposições de longa data em biomecânica e abre portas para inúmeras oportunidades de pesquisa”, disse o autor principal do estudo, Raul Ramos, pesquisador de pós-doutorado no laboratório Plikus para biologia do desenvolvimento e regenerativa. “Direções futuras incluem obter uma compreensão de como os lipocondrócitos mantêm sua estabilidade ao longo do tempo e os programas moleculares que governam sua forma e função, bem como insights sobre os mecanismos do envelhecimento celular. Nossas descobertas ressaltam a versatilidade dos lipídios além do metabolismo e sugerem novas maneiras de aproveitar suas propriedades na engenharia de tecidos e na medicina.”
A equipe incluiu profissionais de saúde e acadêmicos dos EUA, Austrália, Bielorrússia, Dinamarca, Alemanha, Japão, Coreia do Sul e Cingapura, além de funcionários do Serrano Animal & Bird Hospital em Lake Forest e do Zoológico de Santa Ana.
Este trabalho foi apoiado em parte pela Fundação WM Keck sob a bolsa WMKF-5634988; UCI Beall Applied Innovation sob a bolsa Proof of Product IR-PR57179; bolsas da Fundação LEO LF-AW-RAM-19-400008 e LF-OC-20-000611; bolsa da Chan Zuckerberg Initiative AN-0000000062; bolsa Horizon Europe 101137006; Os Institutos Nacionais de Saúde concedem bolsas U01-AR073159, R01- AR079470, R01-AR079150, R21-AR078939, P30-AR075047, R01-AR078389-01, R01-DE015038, R01-AR071457, R01-AR067821, R01GM152494, R01DE030565, TL1-TR001415, R01-DE013828, R01- DE30565, R01-HD073182, R01-AR067797, R01-DE017914 e bolsa de treinamento MBRS-IMSD GM055246; A National Science Foundation concede bolsas DMS1951144, IOS-2421118, DMS1763272, CBET2134916, NSF-GRFP DGE-1321846 e MCB 2028424. Apoio adicional veio da bolsa 594598 da Simons Foundation, da Yoshida Scholarship Foundation, do Howard A. Scheiderman Fellowship Award, da Ben F. Love Chair em Pesquisa do Câncer na Baylor College of Medicine, do Programa de Pós-Doutorado para Professores do Reitor da UC Riverside School of Medicine e da Danish Cancer Society.
Fonte da história:
Materiais fornecidos pela University of California – Irvine . Nota: O conteúdo pode ser editado quanto ao estilo e comprimento.
Multimídia relacionada :
Referência do periódico :
Raul Ramos, Kim T. Pham, Richard C. Prince, Leith B. Leiser-Miller, Maneeshi S. Prasad, Xiaojie Wang, Rachel C. Nordberg, Benjamin J. Bielajew, Jerry C. Hu, Kosuke Yamaga, Ji Won Oh, Tao Peng, Rupsa Datta, Aksana Astrowskaja, Axel A. Almet, John T. Burns, Yuchen Liu, Christian Fernando Guerrero-Juarez, Bryant Q. Tran, Yi-Lin Chu, Anh M. Nguyen, Tsai-Ching Hsi, Norman T.-L. Lim, Sandra Schoeniger, Ruiqi Liu, Yun-Ling Pai, Chella K. Vadivel, Sandy Ingleby, Andrew E. McKechnie, Frank van Breukelen, Kyle L. Hoehn, John J. Rasweiler, Michinori Kohara, William J. Loughry, Scott H. Weldy, Raymond Cosper, Chao-Chun Yang, Sung-Jan Lin, Kimberly L. Cooper, Sharlene E. Santana, Jeffrey E. Bradley, Michael A. Kiebish, Michelle Digman, David E. James, Amy E. Merrill, Qing Nie, Thomas F. Schilling, Aliaksandr A. Astrowski, Eric O. Potma, Martín I. García-Castro, Kyriacos A. Athanasiou, Richard R. Behringer, Maksim V. Plikus. Superstable lipid vacuoles endow cartilage with its shape and biomechanics. Science, 2025; 387 (6730) DOI: 10.1126/science.ads9960